Estados de la materia
Estados de Agregación
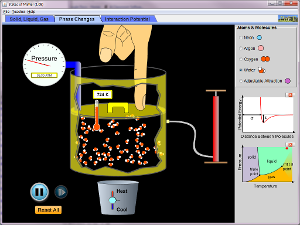
Te invitamos a veas este video para luego continuar:
http://www.wikisaber.es/Contenidos/LObjects/particle_theory/index.html
Teoría de lo visto en el video:
La materia puede aparecer en tres estados de agregación: sólido, líquido y gaseoso.
SÒLIDO
En el estado sólido los cuerpos tienen un volumen casi invariable (incompresibilidad) debido a que sus partículas (átomos, iones o moléculas) están prácticamente en contacto, por lo cual no se pueden aproximar más.
La forma de los sólidos es también invariable, porque sus partículas están perfectamente ordenadas ocupando posiciones fijas en estructuras tridimensionales repetitivas llamadas cristales. Las partículas no están quietas en sus posiciones sino que vibran sin cesar, tanto más intensamente cuanto mayor es la temperatura. Si ésta llega a ser lo suficientemente alta (temperatura de fusión) las partículas pierden sus posiciones fijas y, aunque siguen muy juntas, desaparece la estructura cristalina, exclusiva de los sólidos, para transformarse en líquidos.
Líquido
La forma de los líquidos es variable (adoptan la forma que tiene el recipiente) porque, por encima de la temperatura de fusión, las partículas no pueden mantener las posiciones fijas que tienen en estado sólido y se mueven desordenadamente.Sin el efecto de la gravedad, la forma natural de los líquidos es la esférica (la gota). Si un astronauta, en una estación orbitando la Tierra, lanza un vaso de agua, ésta adopta la forma de grandes gotas suspendidas en el aire.
El volumen de los líquidos es prácticamente invariable, porque las partículas, aunque no forman una estructura fija como en el caso de los sólidos, se mantienen, como en ellos, relativamente juntas.Los líquidos pueden fluir, ya que sus partículas, al tener libertad y no ocupar posiciones fijas, pueden desplazarse por los huecos que aparecen entre ellas, permitiendo el movimiento de toda la masa líquida.
Gaseoso
Los movimientos de las partículas de un líquido se hacen más amplios y rápidos al calentarlo y aumentar su temperatura. Por encima de la temperatura de ebullición, las partículas pierden el contacto entre sí y se mueven libremente en todas direcciones (estado gaseoso).
Los gases se difunden hasta ocupar todo el recipiente que los contiene porque, a diferencia de los sólidos y líquidos, tienen sus partículas muy separadas moviéndose caóticamente en todas direcciones. El movimiento de cada partícula no se verá perturbado mientras no choque con otra partícula o con las paredes del recipiente. Por esta razón, los gases acaban ocupando todo el volumen del recipiente. Los innumerables choques pueden ejercer un empuje tan grande sobre las paredes que éstas pueden llegar a romperse.
La forma de los gases es variable, adoptan la de cualquier recipiente que los contenga.
El volumen de los gases es fácilmente modificable porque se los puede comprimir y expandir.
Presionando un gas se disminuye la separación entre sus partículas, cosa que no puede ocurrir en los estados sólido y líquido.
Los gases pueden fluir, por la misma razón que en el caso de los líquidos. Los líquidos y los gases reciben por ello el nombre genérico de fluidos.
Plasma
Los átomos normalmente están en estado neutro: la carga positiva del núcleo es igual a la carga negativa de los electrones. La agitación de un gas aumenta cuando absorbe calor. Si el calor absorbido es suficiente, los electrones de los átomos son arrancados y la materia queda ionizada, diciéndose que está en estado de plasma. Es plasma todo gas incandescente formado por átomos (a veces moléculas) convertidos en iones positivos y electrones negativos, y todo en continua agitación. Dentro de ese gas pueden quedar también algunos átomos y moléculas sin ionizar (partículas neutras). Ejemplos de gases en estado de plasma son: Algunas zonas de las llamas, el gas de los tubos fluorescentes, el aire que se encuentra en el recorrido de un rayo. La materia que forma las estrellas también está en estado de plasma.
El siguiente texto presenta los distintos estados en que se puede encontrar la materia. Además ofrece una sencilla descripción a nivel molecular de los estados líquidos, sólidos y gaseosos.
Lea el párrafo que aparece abajo y complete las palabras que faltan. Una de las dos palabras que se encuentran entre paréntesis son las correctas)
En el estado (liquido/solido) las partículas que lo forman se unen entre sí por (Fuerzas de atracción/ Fuerzas de repulsión)
En el estado (gaseoso/liquido) las partículas se desplazan por todo el espacio disponible, las fuerzas entre ellas son prácticamente despreciables.
En el estado (liquido/gaseoso) las partículas se desplazan de un lugar a otro, por lo tanto adquiere la forma del recipiente que lo contiene.
La sustancia que pueden hallarse de modo natural en los tres estados, es el
Actividad interactiva para que realices
Debes ingresar y realizar dicha actividad
file:///D:/Plan%2020-30/Quimica/Unidad%202/Comportmacroscopico.htm