Modelos Atómicos
Ahora nos introduciremos en los distintos Modelos Atómicos para luego analizarlos a través de las actividades.
El siguiente texto expone una breve descripción de los distintos modelos atómicos que surgieron a lo largo del tiempo. Además incluye la definición de átomo, molécula, número atómico, masa atómica e isótopo.
Profundizamos:
Teoría atómica de Dalton
En 1808, John Dalton publicó su teoría atómica, que retomaba las antiguas ideas de Leucipo y Demócrito pero basándose en una serie de experiencias científicas de laboratorio.
La teoría atómica de Dalton se basa en los siguientes enunciados:
- La materia está formada por átomos, que son partículas indivisibles e indestructibles.
- Todos los átomos de un mismo elemento químico son iguales en masa y propiedades y diferentes de los átomos de cualquier otro elemento.
- Los compuestos se forman por combinaciones de átomos de diferentes elementos.
Los símbolos de Dalton
Para Dalton, cada elemento está formado una clase de átomos, distinto en sus propiedades a los átomos de los demás elementos y, justamente, es esta distinción lo que separa un elemento de otro y los hace diferentes.
Así, asignó a cada elemento conocido un símbolo distinto, su símbolo químico que con posterioridad ha ido cambiando hasta llegar a los modernos símbolos químicos actuales.
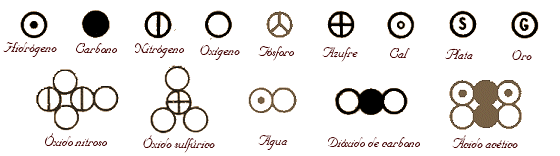
FIGURA 3-3: Símbolos utilizados por Dalton para representar a cada elemento químico.
Enunciados de la Teoría Átomica de Dalton
En 1808 el profesor John Dalton, de nacionalidad Inglesa, formuló la hipótesis sobre la naturaleza de la materia, que se puede resumir en los siguientes enunciados:
- Los elementos están constituidos por partículas diminutas llamadas átomos.
- Todo los átomos de un mismo elemento son idénticos. Hasta que a posterior se descubren los isótopos.
- Los átomos de un elemento dado son diferentes a los de otros elementos.
- Los átomos de un elemento se pueden combinar con los de otro elemento para formar compuestos. En cualquier compuesto, la relación de número de átomos entre dos de los elementos presentes siempre es un número entero.
- Una reacción química incluye solo separación, combinación o reordenamiento de los átomos, nunca se crean o se destruyen.